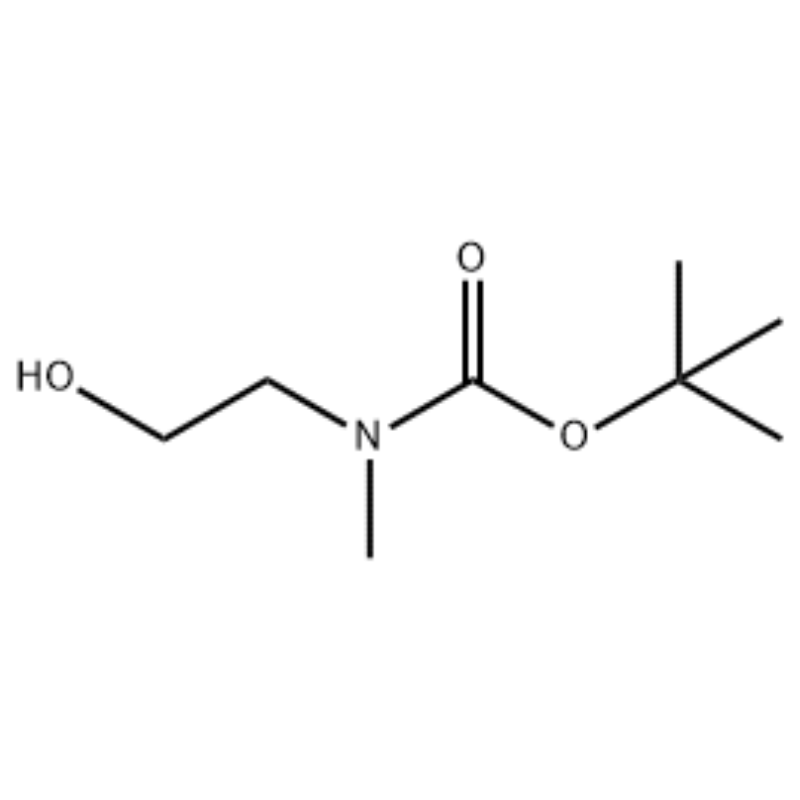
Til en løsning av 2-(metylamino)etanol (500 mg, 0,53 ml, 6,66 mmol) i CH2Cl2 (20 ml) ble det tilsatt Boc2O (1,48 g, 6,79 mmol), etterfulgt av omrøring ved romtemperatur i 1 time.Reaksjonsløsningen ble ekstrahert med saltvann og CH2Cl2.Det således oppnådde organiske laget ble tørket over MgS04 og filtrert.Deretter ble filtratet konsentrert i vakuum for å oppnå den ønskede forbindelse (fargeløs olje, kvantitativ);1H NMR (200 MHz, CDC13) delta 3,74 (q, J= 10,5, 5,2 Hz, 2H) 3,25 (t, J= 5,2 Hz, 2H) 2,91 (s, 3H) 1,45 (s, 9H);massespektrum m/e (relativ intensitet) 144 (20) 102 (24) 57 (70) 44 (100).
Eksempel 38;N1-(3-fluor-4-(2-(1-(2-(metylamino)etyl)-1H-imidazol-4-yl)tieno[3,2-b]pyridin-7-yloksy)fenyl)-N3 -(2-metoksyfenyl)malonamid (96);Trinn 1: tert-butyl-2-hydroksyetyl(metyl)karbamat (97) (J. Med. Chem., 1999, 42, 11, 2008) Til en løsning av 2-(metylamino)etanol (5,0 g, 67 mmol) i THF (50 ml) ved RT ble tilsatt Boc2O (15,7 g, 72 mmol) og reaksjonsblandingen ble omrørt ved RT i 4 timer.Reaksjonsblandingen ble konsentrert til tørrhet og tittelforbindelsen 97 ble brukt direkte i neste trinn uten ytterligere rensing (11,74 g, 100 % utbytte).MS (m/z): 176,2 (M+H).
Fremstilling av l-2-[4-brom-2-(4-okso-2-ftiotaioxo1hiazolidin-5-ylidenmefliyl)fenoksy]efliyl-3-efliyl-l-metylurea(Compoiotamd 161) Trinn 1: Syntese av t-butyl2- hydroksyetylmetylkarbamat;Til en løsning av 2-(metylamino)etanol (500 mg, 0,53 ml, 6,66 mmol) i CH2Cl2 (20 ml) ble det tilsatt BoC2O (1,48 g, 6,79 mmol), etterfulgt av omrøring ved romtemperatur i 1 time.Reaksjonsløsningen ble ekstrahert med saltvann og CH2Cl2.Det således oppnådde organiske laget ble tørket over MgS04 og filtrert.Deretter ble filtratet konsentrert i vakuum for å oppnå den aktuelle forbindelsen (fargeløs olje, kvantitativ); 1HNMR (200 MHz, CDC13) delta 3,74 (q, J= 10,5, 5,2 Hz, 2H) 3,25 (t, J= 5,2 Hz, 2H) 2,91 (s, 3H) 1,45 (s, 9H);massespektrum m/e (relativ intensitet) 144 (20) 102 (24) 57 (70) 44 (100).
2-(metylamino)etanol (90,1 g, 1,2 mol) ble oppløst i 1,2 L metylenklorid, og BoC2O (218 g, 1 mol) ble sakte tilsatt under omrøring ved 0°C, fulgt av ved romtemperatur i 3 timer.Reaksjonsblandingen ble sekvensielt vasket med 700 ml av en vandig løsning av mettet ammoniumklorid og 300 ml vann.Den vaskede blandingen ble dehydrert ved bruk av vannfritt natriumsulfat og konsentrert under redusert trykk for å oppnå forbindelsen (a) (175 g, 1 mol, 100%) som en olje uten farge. TLC: Rf = 0,5 (50% EtOAc i Hex) visualisert med Ce-Mo-farge1H NMR (600MHz, CDC13) delta 1,47 (s, 9H), 2,88 (br s, IH), 3,41 (br s, 2H), 3,76 (br s, 2H).
90,1 g (1,2 mol) 2-(metylamino)etanol ble oppløst i 1,2 L metylenklorid, 218 g (1 mol) Boc2O ble sakte tilsatt mens den resulterende løsningen ble omrørt ved 0C, og den resulterende løsningen ble omrørt ved romtemperatur i 3 timer.Reaksjonsblandingen ble sekvensielt vasket med 700 ml av en vandig mettet ammoniumkloridløsning og 300 ml vann, dehydrert ved bruk av vannfritt natriumsulfat og deretter konsentrert under redusert trykk for å oppnå 175 g (1 mol) av en akromatisk oljeforbindelse beskyttet av Boc-gruppe (utbytte: 100%).[0140] 1H NMR (600 MHz, CDC13) delta 7,84 (br s, 2H), 7,76 (br s, 2H), 4,34 (d, J = 15,0 Hz, 2H), 3,63 (br s, 2H), 3,04 (d , J = 15,0 Hz, 3H), 1,46 (d, J = 16,2 Hz, 9H) [0141] 90 g (0,514 mol) av den oppnådde forbindelsen ble oppløst i 1,5 L tetrahydrofuran, 88,0 g (539 mol) N- hydroksyftalimid og 141 g (0,539 mol) trifenylfosfin ble tilsatt, 106 ml (0,539 mol) diisopropylazodikarboksylat ble sakte tilsatt mens den resulterende løsningen ble omrørt ved 0°C, og den resulterende løsningen ble omrørt i 3 timer mens temperaturen ble hevet. til romtemperatur.Etter konsentrering av reaksjonsblandingen under redusert trykk, ble 600 ml isopropyleter tilsatt, den resulterende løsningen ble omrørt ved 0°C i 1 time, og trifenylfosfinoksyd av hvit fast type ble filtrert.Faststoffet ble vasket med 200 ml isopropyleter avkjølt til 0°C og samlet med det første filtratet, og det resulterende filtratet ble konsentrert under redusert trykk for å oppnå 198 g av en blanding av forbindelse XX og diisopropylhydrazodikarboksylat i et blandingsforhold på 10 til 15 %. (utbytte: 120%).[0142] 1H NMR (600 MHz, CDC13) delta 7,84 (br s, 2H), 7,76 (br s, 2H), 4,34 (d, J = 15,0 Hz, 2H), 3,63 (br s, 2H), 3,04 (d J = 15,0 Hz, 3H), 1,46 (d, J = 16,2 Hz, 9H)
 Building 12, No.309, South 2nd Road, Economic Development Zone, Longquanyi District, Chengdu, Sichuan, Kina.
Building 12, No.309, South 2nd Road, Economic Development Zone, Longquanyi District, Chengdu, Sichuan, Kina. amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com
amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com +86 (028) 84841969
+86 (028) 84841969 +86 135 5885 5404
+86 135 5885 5404



















.png)


